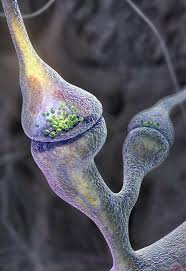
 La sinapsis o articulación interneuronal corresponde a las estructuras que permiten el paso del impulso nervioso desde una célula nerviosa a otra.
La sinapsis o articulación interneuronal corresponde a las estructuras que permiten el paso del impulso nervioso desde una célula nerviosa a otra. Sus componentes son los siguientes:
Superficie presináptica: Generalmente corresponde a una terminal axónica o botón axónico Con la membrana presináptica libre de neurotúbulos y neurofilamentos y donde se aprecian una serie de gránulos, abundantes mitocondrias que permiten el metabolismo aeróbico a este nivel y vesículas sinápticas llenas de neurotransmisor que es sintetizado en el soma y llega a la superficie presináptica a través del flujo axónico anterógrado. Las moléculas que no se liberan vuelven al soma a través del flujo retrógrado.
Espacio sináptico: Mide aprox. 200 Aº. Es el lugar donde se libera el neurotransmisor, el cual cae a la hendidura sináptica y baña la superficie del tercer componente de la sinapsis que es la superficie postsináptica.Tiene material filamentoso y se comunica con el espacio extracelular
Superficie Postsináptica: Es donde el neurotransmisor abre canales iónicos para que comiencen a funcionar los segundos mensajeros, dentro del cuerpo de la segunda neurona. Desencadenando un impulso nervioso
Neurotrasmisores
Los Neurotransmisores son sustancias químicas sintetizadas en el pericarion y almacenadas en los terminales nerviosos en Vesículas Sinápticas. que permiten la transmisión de impulsos nerviosos a nivel de las sinapsis
Otto Loewi el año 1926:
- Aisló y perfundió los corazones de dos ranas controlando la frecuencia cardiaca.
- Estimuló eléctricamente el nervio vago fijado a un corazón, lo cual produjo una disminución de la frecuencia.
- Recogió el líquido que perfundía este corazón y lo transfirió al segundo corazón, disminuyendo en éste la frecuencia, sin haber sido estimulado eléctricamente.
- Con este experimento, dedujo que se había liberado alguna sustancia por la estimulación del nervio vago a partir del corazón estimulado. Denominó a esta sustancia “vagusstoff” y cinco años más tarde mostró que se trataba de la acetilcolina.
Criterios que definen a una sustancia como neurotransmisor:
- La sustancia debe estar presente en el interior de la neurona presináptica.
- La sustancia debe ser liberada en respuesta a la despolarización presináptica, lo cual debe ocurrir en forma de Ca+2 dependiente.
- Se deben presentar receptores específicos en la célula postsináptica.
- Ciclo de vida similar:
- Sintetizadas y empaquetadas en vesículas en la neurona presináptica.
- Liberadas desde la célula presináptica, uniéndose a receptores sobre una o más células postsinápticas.
- Una vez liberadas en la hendidura son eliminadas o degradadas.
- Neuromoduladores actúan sobre la superficie para aumentar o disminuir la cantidad de neurotrasmisores que se liberan.
Aspectos Clínicos de Neurotrasmisores
Por ejemplo la Acetilcolina se libera en la placa motora. En la enfermedad llamada Miastenia, la cantidad de receptores de acetilcolina es muy baja (por problemas inmunológicos, el organismo destruye a los receptores de acetilcolina de la placa motora), por lo tanto, hay debilidad muscular. Para tratar esto, al paciente se le administra Neostigmina, un fármaco que destruye la acetilcolinesterasa (enzima que destruye a la acetilcolina liberada), aumentando en el tiempo el efecto de la acetilcolina liberada en los pocos receptores que quedan.
Además de los neurotransmisores, encontramos a los Neuromoduladores, que corresponden a sustancias que actúan sobre la superficie presináptica, para aumentar o disminuir la cantidad de neurotransmisor que se liberará. Como ejemplos de neuromoduladores tenemos a: encefalinas, endorfinas, Sustancia P, Colecistocinina, Vasopresina, Oxitocina, VIP (péptido intestinal vasoactivo).
- Las funciones anómalas de los neurotransmisores producen una amplia gama de enfermedades psiquiátricas y neurológicas.(Ej : Depresiones, enf. de Parkinson )
- Mejorar las acciones de los neurotransmisores mediante fármacos u otras medidas es fundamental para las terapéuticas modernas.
Tipos de Sinapsis, con relación a los Neurotransmisores:
1. Sinapsis Eléctrica (sin neurotransmisores):
En este tipo, las membranas sinápticas están conectadas directamente. a través de poros o túneles de proteina En ellas, el potencial de acción pasa a la neurona postsináptica sin Retardo ( gap junctions).Existen por ejemplo a nivel de loa sianpasis con llas células musculares lisas Son más abundantes en los animales filogenéticamente más primitivos que el hombre.
2. Sinapsis Electroquímicas:
En este tipo, las membranas no están conectadas, dejan un espacio denominado Hendidura Sináptica.
Entonces La señal que conecta la Neurona Presináptica con una Postsináptica es un Neurotransmisor.
2.1 . Neurotransmisores como:
Los neurotransmisores mas conocidos y mas comunes a nivel del sistema nervioso son: la acetilcolina (ACh), glutamato, ácido gammaaminobutítico (GABA) y glicina.
El neurotransmisor excitatorio mas conocido es el glutamato y los inhibitorios de sinapsis son GABA en el cerebro y la glicina en la médula espinal
Otros neurotransmisores son la norepinefrina (NE), la dopamina (DA) y la serotonina (5HT)
2.2 . Neuromoduladores:
Encefalinas, Endorfinas, Sustancia P, Colecistoquinina, Vasopresina, Oxitocina, Péptidos Intestinales Vasoactivos (VIP).
3. Unión Intermuscular (con neurotransmisores)
Tipos Funcionales de Sinapsis
Las Sinapsis se pueden clasificar en:
Excitatoria: Las membranas postsinápticas reaccionan ante el Neurotransmisor disminuyendo su potencial de reposo, por lo tanto, disminuyendo la negatividad interna, lo que aumenta la excitabilidad.
Inhibitoria: Las membranas postsinápticas se hiperpolariza por el neurotransmisor, por lo que aumenta la negatividad interna, disminuyendo la excitabilidad.
El que una sinapsis sea excitatoria o inhibitoria no depende exclusivamente del neurotransmisor (ya que uno puede actuar indistintamente de las dos formas), sino de las características de la membrana postsinápticas. Los receptores determinan su respuesta ante un neurotransmisor determinado.
Clasificación Estructural de la Sinapsis
Las Sinapsis pueden ocurrir:
Entre Neuronas; Entre una Neurona y una Célula Receptora; Entre una Neurona y una Célula Muscular; Entre una Neurona y una Célula Epitelial.
Según su morfología las sinapsis se clasifican en:
Axodendrítica:
Es el tipo mas frecuente de sinapsis. A medida que el axón se acerca puede tener una expansión terminal (botón terminal) o puede presentar una serie de expansiones (botones de pasaje) cada uno de los cuales hace contacto sináptico.
En este caso las dendritas presentan unas espinas dendríticas y se ha comprobado en ratas que son sometidas a estimulación, que mediante el aprendizaje, aumentan las espinas dendríticas.
Axosomática:
Cuando se une una membrana axónica con el soma de otra membrana.
Axoaxónica :
Son aquellas en que existe un axón que contacta con el segmento inicial de otro axón (donde comienza la vaina de mielina).
Dendrodendrítica
Dendrosomática
Somatosomal
Las tres últimas son exclusivas del Sistema Nervioso Central.
Impulso Nervioso:
La Neurona presenta un Potencial de Reposo, por consecuencia de tener una diferencia de cargas en relación con su medio: en su interior tiene carga negativa (por supremacía de los aniones proteicos junto a iones potasio) y en su exterior positivo (por gran presencia de iones Sodio).
Cuando una neurona es estimulada, su membrana celular pierde su estado de potencial de reposo, por lo tanto, se despolariza dejando el interior celular con carga positiva y el exterior negativo.
Entonces el impulso nervioso es un potencial propagado por el axón desde el soma, tras haber cambiado su polarización ante un estímulo.
_______________________________________________________________________
BIBLIOGRAFÍA
